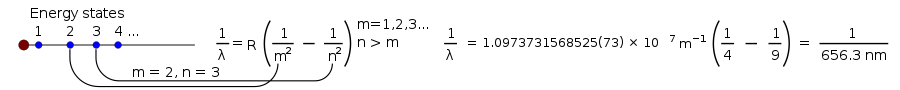Rumus dan gagasan mekanika kuantum dibuat untuk menjelaskan cahaya yang berasal dari hidrogen yang bercahaya. Teori kuantum atom juga harus menjelaskan mengapa elektron tetap berada di orbitnya, yang tidak dapat dijelaskan oleh gagasan lain. Ini mengikuti dari ide-ide yang lebih tua bahwa elektron harus jatuh ke pusat atom karena ia mulai dijaga di orbit oleh energinya sendiri, tetapi dengan cepat akan kehilangan energinya saat ia berputar di orbitnya. (Ini karena elektron dan partikel bermuatan lainnya diketahui memancarkan cahaya dan kehilangan energi ketika mereka mengubah kecepatan atau berbelok).
Lampu hidrogen bekerja seperti lampu neon, tetapi lampu neon memiliki kelompok warna (dan frekuensi) cahayanya sendiri yang unik. Para ilmuwan mengetahui bahwa mereka bisa mengidentifikasi semua elemen dari warna cahaya yang mereka hasilkan. Mereka hanya tidak tahu bagaimana frekuensi ditentukan.
Kemudian, seorang matematikawan Swiss bernama Johann Balmer menemukan persamaan yang memberi tahu berapa λ (lambda, untuk panjang gelombang):
λ = B ( n 2 n 2 - 4 ) n = 3 , 4 , 5 , 6 {\displaystyle \lambda =B\kiri({\frac {n^{{2}}{n^{2}-4}}}\kanan)\qquad \qquad n=3,4,5,6} 
di mana B adalah angka yang ditentukan Balmer sama dengan 364,56 nm.
Persamaan ini hanya bekerja untuk cahaya tampak dari lampu hidrogen. Tetapi kemudian, persamaan itu dibuat lebih umum:
1 λ = R ( 1 m 2 - 1 n 2 ) , {\displaystyle {\frac {1}{{\lambda }}=R\left({\frac {1}{m^{2}}}}-{\frac {1}{n^{2}}}}}}}}}\right),} 
di mana R adalah konstanta Rydberg, sama dengan 0,0110 nm−1 , dan n harus lebih besar dari m.
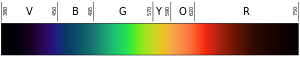
Dengan memasukkan angka-angka yang berbeda untuk m dan n, mudah untuk memprediksi frekuensi untuk banyak jenis cahaya (ultraviolet, tampak, dan infared). Untuk melihat bagaimana cara kerjanya, buka Hyperphysics dan turun melewati bagian tengah halaman. (Gunakan H = 1 untuk hidrogen).
Pada tahun 1908, Walter Ritz membuat prinsip kombinasi Ritz yang menunjukkan bagaimana celah tertentu di antara frekuensi terus berulang. Hal ini ternyata penting bagi Werner Heisenberg beberapa tahun kemudian.
Pada tahun 1905, Albert Einstein menggunakan ide Planck untuk menunjukkan bahwa seberkas cahaya terdiri dari aliran partikel yang disebut foton. Energi setiap foton tergantung pada frekuensinya. Gagasan Einstein adalah awal dari gagasan dalam mekanika kuantum bahwa semua partikel subatomik seperti elektron, proton, neutron, dan lainnya adalah gelombang dan partikel pada saat yang sama. (Lihat gambar atom dengan elektron sebagai gelombang pada atom.) Hal ini menyebabkan teori tentang partikel subatomik dan gelombang elektromagnetik yang disebut dualitas gelombang-partikel. Di sinilah partikel dan gelombang tidak satu atau yang lain, tetapi memiliki sifat tertentu dari keduanya.
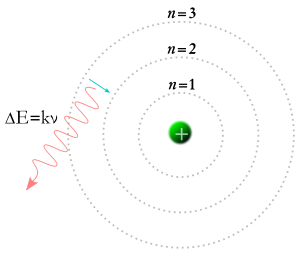
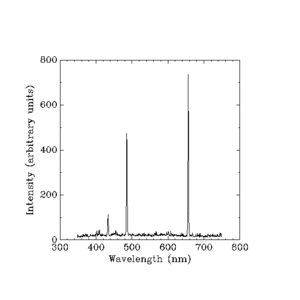
Pada tahun 1913, Niels Bohr muncul dengan gagasan bahwa elektron hanya dapat mengambil orbit tertentu di sekitar inti atom. Di bawah teori Bohr, angka-angka yang disebut m dan n dalam persamaan di atas dapat mewakili orbit. Teori Bohr mengatakan elektron bisa mulai di beberapa orbit m dan berakhir di beberapa orbit n, atau elektron bisa mulai di beberapa orbit n dan berakhir di beberapa orbit m jadi jika sebuah foton mengenai elektron, energinya akan diserap, dan elektron akan pindah ke orbit yang lebih tinggi karena energi ekstra itu. Berdasarkan teori Bohr, jika elektron jatuh dari orbit yang lebih tinggi ke orbit yang lebih rendah, maka elektron harus menyerahkan energi dalam bentuk foton. Energi foton akan sama dengan perbedaan energi antara kedua orbit, dan energi foton membuatnya memiliki frekuensi dan warna tertentu. Teori Bohr memberikan penjelasan yang baik tentang banyak aspek fenomena subatomik, tetapi gagal menjawab mengapa masing-masing warna cahaya yang dihasilkan oleh hidrogen yang bercahaya (dan oleh neon yang bercahaya atau elemen lainnya) memiliki kecerahannya sendiri, dan perbedaan kecerahan selalu sama untuk setiap elemen.
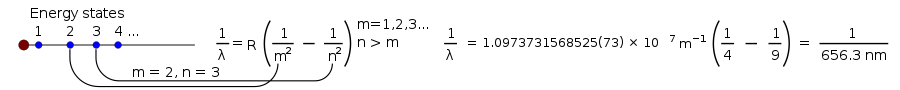
Pada saat Niels Bohr mengeluarkan teorinya, sebagian besar hal tentang cahaya yang dihasilkan oleh lampu hidrogen sudah diketahui, tetapi para ilmuwan masih belum bisa menjelaskan kecerahan setiap garis yang dihasilkan oleh hidrogen yang bersinar.
Werner Heisenberg mengambil tugas untuk menjelaskan kecerahan atau "intensitas" dari setiap garis. Dia tidak bisa menggunakan aturan sederhana seperti yang dibuat oleh Balmer. Dia harus menggunakan matematika fisika klasik yang sangat sulit yang menghitung semuanya dalam hal hal-hal seperti massa (berat) elektron, muatan (kekuatan listrik statis) elektron, dan jumlah kecil lainnya. Fisika klasik sudah memiliki jawaban untuk kecerahan pita warna yang dihasilkan lampu hidrogen, tetapi teori klasik mengatakan bahwa harus ada pelangi yang berkelanjutan, dan bukan empat pita warna yang terpisah. Penjelasan Heisenberg adalah:
Ada beberapa hukum yang mengatakan frekuensi cahaya apa yang akan dihasilkan oleh hidrogen yang bercahaya. Ini harus memprediksi frekuensi yang berjarak ketika elektron yang terlibat bergerak di antara orbit yang dekat dengan inti (pusat) atom, tetapi juga harus memprediksi bahwa frekuensi akan semakin dekat dan lebih dekat bersama ketika kita melihat apa yang dilakukan elektron dalam bergerak di antara orbit semakin jauh dan semakin jauh keluar. Ini juga akan memprediksi bahwa perbedaan intensitas antara frekuensi semakin dekat dan semakin dekat bersama saat kita keluar. Ketika fisika klasik sudah memberikan jawaban yang benar dengan satu set persamaan, fisika baru harus memberikan jawaban yang sama tetapi dengan persamaan yang berbeda.
Fisika klasik menggunakan metode matematikawan Prancis Fourier untuk membuat gambaran matematika dari dunia fisik, dan menggunakan kumpulan kurva halus yang menyatu untuk membuat satu kurva halus yang memberikan, dalam hal ini, intensitas untuk cahaya dari semua frekuensi dari beberapa cahaya. Tapi itu tidak benar karena kurva halus itu hanya muncul pada frekuensi yang lebih tinggi. Pada frekuensi yang lebih rendah, selalu ada titik-titik yang terisolasi dan tidak ada yang menghubungkan titik-titik tersebut. Jadi, untuk membuat peta dunia nyata, Heisenberg harus membuat perubahan besar. Dia harus melakukan sesuatu untuk memilih hanya angka-angka yang cocok dengan apa yang terlihat di alam. Kadang-kadang orang mengatakan dia "menebak" persamaan-persamaan ini, tetapi dia tidak membuat tebakan buta. Dia menemukan apa yang dia butuhkan. Angka-angka yang dia hitung akan menempatkan titik-titik pada grafik, tetapi tidak akan ada garis yang ditarik di antara titik-titik itu. Dan membuat satu "grafik" hanya dari titik-titik untuk setiap rangkaian perhitungan akan membuang banyak kertas dan tidak akan menyelesaikan apa pun. Heisenberg menemukan cara untuk memprediksi intensitas secara efisien untuk frekuensi yang berbeda dan untuk mengatur informasi itu dengan cara yang bermanfaat.
Hanya dengan menggunakan aturan empiris yang diberikan di atas, aturan yang dimulai oleh Balmer dan diperbaiki oleh Rydberg, kita dapat melihat bagaimana mendapatkan satu set angka yang akan membantu Heisenberg mendapatkan jenis gambar yang diinginkannya:
Aturannya mengatakan bahwa ketika elektron bergerak dari satu orbit ke orbit lainnya, ia akan memperoleh atau kehilangan energi, tergantung pada apakah ia semakin jauh dari pusat atau lebih dekat dengannya. Jadi, kita dapat menempatkan orbit atau tingkat energi ini sebagai judul di sepanjang bagian atas dan samping kisi. Untuk alasan historis, orbit terendah disebut n, dan orbit berikutnya disebut n - a, kemudian muncul n - b, dan seterusnya. Memang membingungkan bahwa mereka menggunakan angka negatif ketika elektron sebenarnya mendapatkan energi, tetapi begitulah adanya.
Karena aturan Rydberg memberi kita frekuensi, kita dapat menggunakan aturan itu untuk memasukkan angka tergantung ke mana elektron pergi. Jika elektron mulai dari n dan berakhir di n, maka elektron tidak benar-benar pergi ke mana pun, jadi ia tidak mendapatkan energi dan tidak kehilangan energi. Jadi frekuensinya adalah 0. Jika elektron mulai dari n-a dan berakhir di n, maka ia telah jatuh dari orbit yang lebih tinggi ke orbit yang lebih rendah. Jika hal itu terjadi, maka ia kehilangan energi, dan energi yang hilang muncul sebagai foton. Foton memiliki sejumlah energi, e, dan itu terkait dengan frekuensi tertentu f dengan persamaan e = h f. Jadi kita tahu bahwa perubahan orbit tertentu akan menghasilkan frekuensi cahaya tertentu, f. Jika elektron mulai dari n dan berakhir di n - a, itu berarti ia telah berpindah dari orbit yang lebih rendah ke orbit yang lebih tinggi. Itu hanya terjadi ketika foton dengan frekuensi dan energi tertentu masuk dari luar, diserap oleh elektron dan memberinya energi, dan itulah yang membuat elektron keluar ke orbit yang lebih tinggi. Jadi, agar semuanya masuk akal, kita menulis frekuensi itu sebagai angka negatif. Ada foton dengan frekuensi tertentu dan sekarang telah diambil.
Jadi kita bisa membuat kisi-kisi seperti ini, di mana f(a←b) berarti frekuensi yang terlibat ketika elektron berpindah dari keadaan energi (orbit) b ke keadaan energi a (Sekali lagi, urutannya terlihat terbalik, tetapi begitulah cara awalnya ditulis.):
Kisi-kisi dari f
| Keadaan Elektron | n | n-a | n-b | n-c | .... | |
| n | f(n←n) | f(n←n-a) | f(n←n-b) | f(n←n-c) | ..... | |
| n-a | f(n-a←n) | f(n-a←n-a) | f(n-a←n-b) | f(n-a←n-c) | ..... | |
| n-b | f(n-b←n) | f(n-b←n-a) | f(n-b←n-b) | f(n-b←n-c) | ..... | |
| transisi.... | ..... | ..... | ..... | ..... | | |
Heisenberg tidak membuat kisi-kisi seperti ini. Dia hanya melakukan perhitungan yang memungkinkannya mendapatkan intensitas yang dia cari. Tetapi untuk melakukan itu, dia harus mengalikan dua amplitudo (seberapa tinggi ukuran gelombang) untuk mengetahui intensitasnya. (Dalam fisika klasik, intensitas sama dengan amplitudo kuadrat.) Dia membuat persamaan yang tampak aneh untuk menangani masalah ini, menulis sisa makalahnya, menyerahkannya kepada atasannya, dan pergi berlibur. Dr. Born melihat persamaan lucunya dan itu tampak sedikit gila. Dia pasti bertanya-tanya, "Mengapa Heisenberg memberi saya hal yang aneh ini? Mengapa dia harus melakukannya dengan cara ini?" Kemudian dia menyadari bahwa dia sedang melihat cetak biru untuk sesuatu yang sudah dia ketahui dengan sangat baik. Dia terbiasa menyebut kisi-kisi atau tabel yang bisa kita tulis dengan melakukan, misalnya, semua matematika untuk frekuensi, matriks. Dan persamaan aneh Heisenberg adalah aturan untuk mengalikan dua dari mereka bersama-sama. Max Born adalah seorang matematikawan yang sangat, sangat baik. Dia tahu bahwa karena dua matriks (kisi-kisi) yang dikalikan mewakili hal-hal yang berbeda (seperti posisi (x,y,z) dan momentum (mv), misalnya), maka ketika Anda mengalikan matriks pertama dengan matriks kedua, Anda akan mendapatkan satu jawaban, dan ketika Anda mengalikan matriks kedua dengan matriks pertama, Anda akan mendapatkan jawaban yang lain. Meskipun dia tidak tahu tentang matematika matriks, Heisenberg sudah melihat masalah "jawaban yang berbeda" ini dan itu telah mengganggunya. Born adalah seorang matematikawan yang baik sehingga dia melihat bahwa perbedaan antara perkalian matriks pertama dan perkalian matriks kedua selalu akan melibatkan konstanta Planck, h, dikalikan dengan akar kuadrat dari negatif satu, i. Jadi dalam beberapa hari setelah penemuan Heisenberg, mereka sudah memiliki matematika dasar untuk apa yang Heisenberg suka menyebutnya "prinsip ketidakpastian". Dengan "tak tentu" Heisenberg berarti bahwa sesuatu seperti elektron tidak dijepit sampai dijepit. Ini sedikit seperti ubur-ubur yang selalu meremas-remas dan tidak bisa "di satu tempat" kecuali Anda membunuhnya. Belakangan, orang terbiasa menyebutnya "prinsip ketidakpastian Heisenberg," yang membuat banyak orang membuat kesalahan dengan berpikir bahwa elektron dan hal-hal seperti itu benar-benar "ada di suatu tempat" tetapi kita hanya tidak yakin tentang hal itu dalam pikiran kita sendiri. Gagasan itu salah. Bukan itu yang dibicarakan Heisenberg. Mengalami kesulitan mengukur sesuatu adalah masalah, tetapi itu bukan masalah yang dibicarakan Heisenberg.
Gagasan Heisenberg sangat sulit dipahami, tetapi kita dapat membuatnya lebih jelas dengan sebuah contoh. Pertama, kita akan mulai menyebut kisi-kisi ini sebagai "matriks," karena kita akan segera perlu berbicara tentang perkalian matriks.
Misalkan kita mulai dengan dua jenis pengukuran, posisi (q) dan momentum (p). Pada tahun 1925, Heisenberg menulis persamaan seperti ini:
Y ( n , n - b ) = ∑ a p ( n , n - a ) q ( n - a , n - b ) {\displaystyle Y(n,n - b)=\sum _{a}^{}}\,p(n,n - a)q(n - a,n - b)} (Persamaan untuk variabel konjugat momentum dan posisi)
(Persamaan untuk variabel konjugat momentum dan posisi)
Dia tidak mengetahuinya, tetapi persamaan ini memberikan cetak biru untuk menuliskan dua matriks (kisi-kisi) dan untuk mengalikannya. Aturan untuk mengalikan satu matriks dengan matriks lainnya sedikit berantakan, tetapi berikut ini adalah dua matriks menurut cetak biru tersebut, dan kemudian hasil kalinya:
Matriks dari p
| Keadaan Elektron | n-a | n-b | n-c | .... | |
| n | p(n←n-a) | p(n←n-b) | p(n←n-c) | ..... | |
| n-a | p(n-a←n-a) | p(n-a←n-b) | p(n-a←n-c) | ..... | |
| n-b | p(n-b←n-a) | p(n-b←n-b) | p(n-b←n-c) | ..... | |
| transisi.... | ..... | ..... | ..... | ..... | |
Matriks dari q
| Keadaan Elektron | n-b | n-c | n-d | .... | |
| n-a | q(n-a←n-b) | q(n-a←n-c) | q(n-a←n-d) | ..... | |
| n-b | q(n-b←n-b) | q(n-b←n-c) | q(n-b←n-d) | ..... | |
| n-c | q(n-c←n-b) | q(n-c←n-c) | q(n-c←n-d) | ..... | |
| transisi.... | ..... | ..... | ..... | ..... | |
Matriks untuk hasil kali dua matriks di atas seperti yang ditentukan oleh persamaan yang relevan dalam makalah Heisenberg tahun 1925 adalah:
| Keadaan Elektron | n-b | n-c | n-d | ..... |
| n | A | ..... | ..... | ..... |
| n-a | ..... | B | ..... | ..... |
| n-b | ..... | ..... | C | ..... |
Di mana:
A=p(n←n-a)*q(n-a←n-b)+p(n←n-b)*q(n-b←n-b)+p(n←n-c)*q(n-c←n-b)+.....
B=p(n-a←n-a)*q(n-a←n-c)+p(n-a←n-b)*q(n-b←n-c)+p(n-a←n-c)*q(n-c←n-c)+.....
C=p(n-b←n-a)*q(n-a←n-d)+p(n-b←n-b)*q(n-b←n-d)+p(n-b←n-c)*q(n-d←n-d)+.....
dan sebagainya.
Jika matriks-matriks itu dibalik, nilai-nilai berikut ini akan dihasilkan:
A=q(n←n-a)*p(n-a←n-b)+q(n←n-b)*p(n-b←n-b)+q(n←n-c)*p(n-c←n-b)+.....
B=q(n-a←n-a)*p(n-a←n-c)+q(n-a←n-b)*p(n-b←n-c)+q(n-a←n-c)*p(n-c←n-c)+.....
C=q(n-b←n-a)*p(n-a←n-d)+q(n-b←n-b)*p(n-b←n-d)+q(n-b←n-c)*p(n-d←n-d)+.....
dan sebagainya.
Perhatikan bagaimana mengubah urutan perkalian mengubah angka-angka, langkah demi langkah, yang sebenarnya dikalikan.