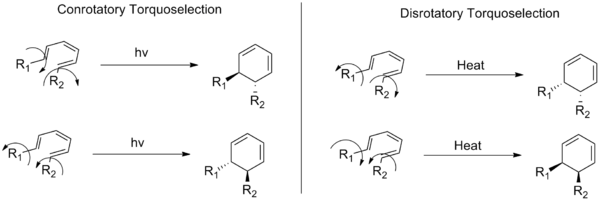
Istilah-istilah ini menggambarkan dua kelas reaksi elektrosiklik (sejenis reaksi kimia organik). Dalam mode konrotatori, substituen yang terletak di ujung sistem ikatan rangkap terkonjugasi bergerak ke arah yang sama (searah jarum jam atau berlawanan arah jarum jam) selama pembukaan cincin atau penutupan cincin. Dalam mode disrotatori, mereka bergerak ke arah yang berlawanan.
Contohnya adalah konversi trans-cis-trans-2,4,6-oktatriena menjadi cis-dimethylcyclohexadiene (bagian atas gambar). Mekanika orbital dari reaksi membutuhkan mode disrotatori. Simetri orbital dari orbital molekul tertinggi yang ditempati octatriene (HOMO) mengharuskan orbital pi akhir untuk bergerak ke arah yang berlawanan untuk membentuk simetri yang benar yang ditemukan dalam ikatan sigma.
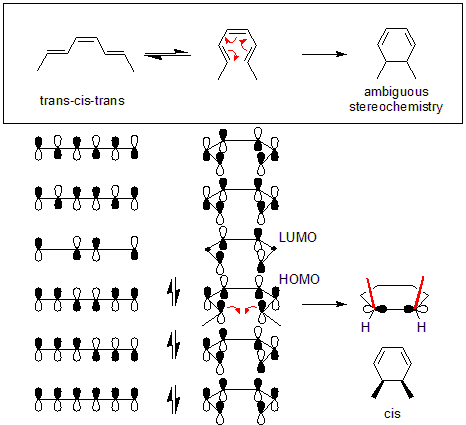
Penataan ulang termal dari semua sistem terkonjugasi yang mengandung elektron 4n + 2 pi bersifat stereospesifik. Hal ini didasarkan pada pelestarian simetri orbital dalam orbital molekul tertinggi yang ditempati. Sistem yang mengandung elektron 4n pi menunjukkan mode konrotasi yang berlawanan. Hal ini juga berlaku untuk penataan ulang elektron 4n + 2 pi (di mana n adalah bilangan bulat) yang digerakkan oleh cahaya (photoinduced). Penataan ulang yang diinduksi foto dari sistem elektron 4n pi (di mana jumlah elektron dapat dibagi 4) mengikuti aturan disrotatori.
Aturan Woodward-Hoffmann merangkum reaksi-reaksi berbeda di atas.
Gambar berikut ini juga menunjukkan perbedaan antara reaksi konrotatori dan disrotatori: