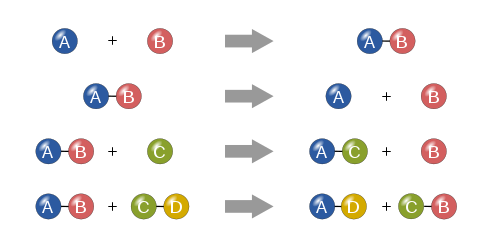
Sintesis
Dalam reaksi sintesis, dua atau lebih zat sederhana bergabung untuk membentuk zat yang lebih kompleks.
A + B ⟶ A B {\displaystyle A+B\longrightarrow AB} 
"Dua reaktan atau lebih yang menghasilkan satu produk" adalah cara lain untuk mengidentifikasi reaksi sintesis. Salah satu contoh reaksi sintesis adalah kombinasi besi dan belerang untuk membentuk besi (II) sulfida:
8 F e + S 8 ⟶ 8 F e S {\displaystyle 8Fe+S_{8}\longrightarrow 8FeS} 
Contoh lainnya adalah gas hidrogen sederhana yang dikombinasikan dengan gas oksigen sederhana untuk menghasilkan zat yang lebih kompleks, seperti air.
Dekomposisi
Reaksi dekomposisi adalah ketika zat yang lebih kompleks terurai menjadi bagian-bagiannya yang lebih sederhana. Dengan demikian, ini adalah kebalikan dari reaksi sintesis, dan dapat ditulis sebagai:
A B ⟶ A + B {\displaystyle AB\longrightarrow A+B} 
Salah satu contoh reaksi dekomposisi adalah elektrolisis air untuk membuat gas oksigen dan hidrogen:
2 H 2 O ⟶ 2 H 2 + O 2 {\displaystyle 2H_{2}O\longrightarrow 2H_{2}+O_{2}} 
Penggantian tunggal
Dalam reaksi penggantian tunggal, satu elemen yang tidak digabungkan menggantikan elemen lain dalam suatu senyawa; dengan kata lain, satu elemen bertukar tempat dengan elemen lain dalam suatu senyawa Reaksi-reaksi ini datang dalam bentuk umum:
A + B C ⟶ A C + B {\displaystyle A+BC\longrightarrow AC+B} 
Salah satu contoh reaksi perpindahan tunggal adalah ketika magnesium menggantikan hidrogen dalam air untuk membuat magnesium hidroksida dan gas hidrogen:
M g + 2 H 2 O ⟶ M g ( O H ) 2 + H 2 {\displaystyle Mg+2H_{2}O\longrightarrow Mg(OH)_{2}+H_{2}}} 
Penggantian ganda
Dalam reaksi penggantian ganda, anion dan kation dari dua senyawa bertukar tempat dan membentuk dua senyawa yang sama sekali berbeda. Reaksi-reaksi ini dalam bentuk umum:
A B + C D ⟶ A D + C B {\gaya tampilan AB+CD\gaya tampilan AD+CB} 
Misalnya, ketika barium klorida (BaCl2 ) dan magnesium sulfat (MgSO4 ) bereaksi, anion SO42− bertukar tempat dengan anion 2Cl− , menghasilkan senyawa BaSO4 dan MgCl2 .
Contoh lain dari reaksi perpindahan ganda adalah reaksi timbal (II) nitrat dengan kalium iodida untuk membentuk timbal (II) iodida dan kalium nitrat:
P b ( N O 3 ) 2 + 2 K I ⟶ P b I 2 + 2 K N O 3 {\displaystyle Pb(NO_{3})_{2}+2KI\longrightarrow PbI_{2}+2KNO_{3}}}