Cangkang elektron
Kulit elektron adalah bagian luar atom di sekitar inti atom. Ini adalah tempat elektron berada, dan merupakan sekelompok orbital atom dengan nilai yang sama dari bilangan kuantum utama n.
Kulit elektron memiliki satu atau lebih subkulit elektron, atau sublevel. Sublevel-sublevel ini memiliki dua atau lebih orbital dengan bilangan kuantum momentum sudut yang sama l. Cangkang elektron membentuk konfigurasi elektron suatu atom. Jumlah elektron yang bisa berada dalam cangkang sama dengan 2 n 2 {\displaystyle 2n^{{2}}. 
Nama untuk kulit elektron berasal dari model Bohr, di mana kelompok elektron diyakini mengelilingi nukleus pada jarak tertentu, sehingga orbit mereka membentuk "cangkang". Istilah ini dikemukakan oleh dokter Denmark Niels Henrik David Bohr.
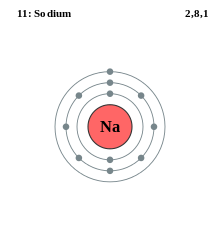
Contoh model kulit elektron natrium yang memiliki tiga kulit
Cangkang valensi
Cangkang valensi adalah cangkang terluar dari atom dalam keadaan tidak digabungkan, yang mengandung elektron yang paling mungkin untuk menjelaskan sifat dari setiap reaksi yang melibatkan atom dan interaksi ikatan yang dimilikinya dengan atom lain. Harus diperhatikan bahwa kulit terluar dari suatu ion tidak biasa disebut kulit valensi. Elektron dalam kulit valensi disebut sebagai elektron valensi.
Dalam gas mulia, sebuah atom cenderung memiliki 8 elektron di kulit terluarnya (kecuali helium, yang hanya mampu mengisi kulitnya dengan 2 elektron). Ini berfungsi sebagai model untuk aturan oktet yang sebagian besar berlaku untuk elemen-elemen kelompok utama periode kedua dan ketiga. Dalam hal orbital atom, elektron-elektron dalam kulit valensi didistribusikan 2 dalam orbital s tunggal dan masing-masing 2 dalam tiga orbital p.
Untuk kompleks koordinasi yang mengandung logam transisi, kulit valensi terdiri dari elektron dalam orbital s dan p ini, serta hingga 10 elektron tambahan, didistribusikan sebagai 2 ke masing-masing dari 5 orbital d, untuk membuat total 18 elektron dalam cangkang valensi lengkap untuk senyawa semacam itu. Ini disebut sebagai aturan delapan belas elektron.
| Kemungkinan Jumlah Elektron dalam cangkang 1-5 | |
| Shell | Elektron |
| 1 | 2 |
| 2 | 8 |
| 3 | 18 |
| 4 | 32 |
| 5 | 32 |
| 6 | 18 |
| 7 | 8 |
Subshells
Sub kulit elektron diidentifikasi dengan huruf s, p, d, f, g, h, i, dll., Sesuai dengan bilangan kuantum azimuthal (nilai-l) 0, 1, 2, 3, 4, 5, 6, dll. Setiap kulit dapat menampung hingga 2, 6, 10, 14, dan 18 elektron masing-masing, atau 2(2l + 1) elektron di setiap subshell. Notasi 's', 'p', 'd', dan 'f' berasal dari sistem yang sekarang didiskreditkan untuk mengkategorikan garis spektral sebagai "tajam", "utama", "menyebar", atau "fundamental", berdasarkan struktur halus yang diamati. Ketika empat jenis orbital pertama dideskripsikan, mereka dikaitkan dengan jenis garis spektral ini, tetapi tidak ada nama lain. Sebutan 'g', 'h', dan seterusnya, diturunkan dengan mengikuti urutan abjad.
Pertanyaan dan Jawaban
T: Apa yang dimaksud dengan kulit elektron?
J: Cangkang elektron, atau tingkat energi utama, adalah bagian dari atom di mana elektron ditemukan mengorbit inti atom.
T: Berapa banyak elektron yang bisa berada dalam cangkang tertentu?
A: Jumlah elektron yang bisa berada dalam cangkang tertentu sama dengan 2n2.
T: Apa yang dinyatakan oleh model Bohr tentang elektron?
J: Model Bohr menyatakan bahwa elektron-elektron mengorbit nukleus pada jarak-jarak tertentu sehingga orbitnya membentuk "cangkang".
T: Siapa yang mempresentasikan istilah ini?
J: Istilah ini dipresentasikan oleh Niels Henrik David Bohr.
T: Apa yang membentuk konfigurasi elektron dari sebuah atom?
A: Cangkang elektron membentuk konfigurasi elektron suatu atom.
T: Apakah semua atom terdiri dari satu atau lebih kulit elektron?
A: Ya, semua atom memiliki satu atau lebih kulit elektron.
T: Apakah semua kulit elektron memiliki jumlah elektron yang bervariasi?
J: Ya, semua kulit elektron memiliki jumlah elektron yang bervariasi.
Cari di dalam ensiklopedia