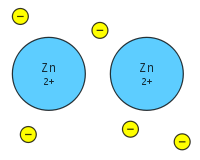
Ikatan logam adalah pembagian banyak elektron yang terlepas di antara banyak ion positif, di mana elektron bertindak sebagai "lem" yang memberi zat struktur yang pasti. Ini tidak seperti ikatan kovalen atau ionik. Logam memiliki energi ionisasi yang rendah. Oleh karena itu, elektron valensi dapat terdelokalisasi di seluruh logam. Elektron yang terdelokalisasi tidak terkait dengan inti logam tertentu, sebaliknya, elektron bebas bergerak ke seluruh struktur kristal membentuk "lautan" elektron.
Elektron dan ion positif dalam logam memiliki gaya tarik-menarik yang kuat di antara mereka. Oleh karena itu, logam sering kali memiliki titik leleh atau titik didih yang tinggi. Prinsipnya mirip dengan ikatan ionik.
Ikatan logam menyebabkan banyak sifat logam, seperti kekuatan, kelenturan, keuletan, kilau, konduksi panas dan listrik.
Karena elektron bergerak bebas, logam memiliki konduktivitas listrik. Ini memungkinkan energi untuk melewati elektron dengan cepat, menghasilkan arus listrik. Logam menghantarkan panas untuk alasan yang sama: elektron bebas dapat mentransfer energi pada tingkat yang lebih cepat daripada zat lain dengan elektron yang tetap pada posisinya. Ada juga beberapa non-logam yang menghantarkan listrik: grafit (karena, seperti logam, ia memiliki elektron bebas), dan senyawa ionik yang cair atau terlarut dalam air, yang memiliki ion yang bergerak bebas.
Ikatan logam memiliki setidaknya satu elektron valensi yang tidak mereka bagi dengan atom tetangga, dan mereka tidak kehilangan elektron untuk membentuk ion. Sebaliknya, tingkat energi luar (orbital atom) dari atom logam tumpang tindih. Mereka mirip dengan ikatan kovalen. Tidak semua logam menunjukkan ikatan logam. Misalnya, ion merkuri (Hg2+
2 ) membentuk ikatan logam-logam kovalen.
Paduan adalah larutan logam. Sebagian besar paduan mengkilap seperti logam murni.