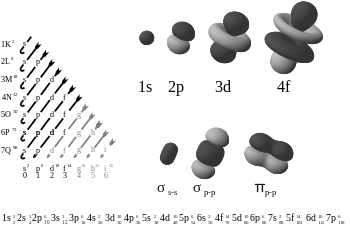
Dalam kimia, ikatan pi (ikatan π) adalah ikatan kimia kovalen di mana jalur orbital satu elektron bersilangan (tumpang tindih) dengan jalur elektron lainnya. Elektron-elektron memiliki jalur berbentuk lobus angka delapan (lihat gambar). Ada dua area tumpang tindih karena jalurnya tumpang tindih pada kedua lobus. Hanya satu dari bidang nodal orbital yang melewati kedua inti yang terlibat.
Huruf Yunani π dalam nama mereka mengacu pada orbital p. Simetri orbital dari ikatan pi terlihat sama dengan orbital p ketika dilihat ke bawah sumbu ikatan. Orbital p biasanya memiliki ikatan semacam ini. Orbital D juga diasumsikan menggunakan ikatan pi tetapi ini belum tentu apa yang terjadi dalam kenyataan. Ide ikatan orbital d cocok dengan teori hipervalensi.
Ikatan pi biasanya lebih lemah dari ikatan sigma. Mekanika kuantum mengatakan ini karena jalur orbitalnya paralel sehingga ada lebih sedikit tumpang tindih antara orbital-p.
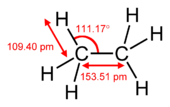
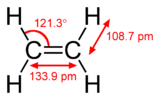
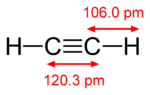
Ikatan Pi terjadi ketika dua orbital atom bersentuhan melalui dua area tumpang tindih. Ikatan pi adalah ikatan yang lebih menyebar daripada ikatan sigma. Elektron dalam ikatan pi kadang-kadang disebut elektron pi. Fragmen molekul yang bergabung dengan ikatan pi tidak dapat berotasi tentang ikatan itu tanpa memutus ikatan pi. Rotasi menghancurkan jalur paralel dari dua orbital p.