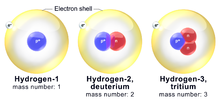
Atom-atom unsur kimia bisa ada dalam berbagai jenis. Ini disebut isotop. Mereka memiliki jumlah proton (dan elektron) yang sama, tetapi jumlah neutron yang berbeda. Isotop yang berbeda dari unsur yang sama memiliki massa yang berbeda. Massa adalah kata untuk berapa banyak zat (atau materi) yang dimiliki sesuatu. Sesuatu dengan massa yang berbeda memiliki bobot yang berbeda. Karena isotop-isotop yang berbeda memiliki jumlah neutron yang berbeda, maka beratnya tidak semuanya sama atau memiliki massa yang sama.
Isotop yang berbeda dari unsur yang sama memiliki nomor atom yang sama. Mereka memiliki jumlah proton yang sama. Nomor atom ditentukan oleh jumlah proton. Isotop memiliki nomor massa yang berbeda, karena mereka memiliki jumlah neutron yang berbeda.
Kata isotop, yang berarti di tempat yang sama, berasal dari fakta bahwa isotop berada di tempat yang sama pada tabel periodik.
Dalam atom netral, jumlah elektron sama dengan jumlah proton. Isotop dari unsur yang sama juga memiliki jumlah elektron dan struktur elektronik yang sama. Karena bagaimana atom bertindak ditentukan oleh struktur elektroniknya, isotop hampir sama secara kimiawi, tetapi berbeda secara fisik dengan atom aslinya.
Isotop yang lebih berat bereaksi lebih lambat secara kimiawi daripada isotop yang lebih ringan dari unsur yang sama. "Efek massa" ini lebih besar untuk protium (1 H) dan deuterium (2 H), karena deuterium memiliki dua kali massa protium. Untuk unsur yang lebih berat, rasio berat atom relatif antara isotop jauh lebih sedikit, dan efek massa biasanya kecil.